新研究發(fā)現(xiàn)散發(fā)性阿爾茨海默病深層致病機制
新華社耶路撒冷10月5日電(記者王卓倫)以色列理工學院近日發(fā)布公報說,,其研究人員領(lǐng)銜的一個國際團隊發(fā)現(xiàn),,散發(fā)性阿爾茨海默病患者大腦中有毒蛋白質(zhì)的積累與蛋白質(zhì)清除機制失效有關(guān),靶向特定蛋白或可緩解病癥,。相關(guān)論文發(fā)表在英國《自然·通訊》雜志上,。
公報說,阿爾茨海默病在65歲以上人群中高發(fā),,其特點為隨著腦神經(jīng)細胞的退化和死亡,,人的認知能力逐漸下降。這一疾病分為家族性和散發(fā)性,,特征均為大腦中有毒蛋白質(zhì)的積累,。前者與基因突變引起的相關(guān)蛋白質(zhì)積累有關(guān),而在更普遍的散發(fā)性阿爾茨海默病中,,有毒蛋白質(zhì)積累的觸發(fā)機制尚不清楚。
研究人員提出了一種假設,,即大腦中有毒蛋白質(zhì)的積累是由蛋白質(zhì)清除機制(又稱為泛素-蛋白酶體系統(tǒng))失效造成,。泛素是存在于所有真核生物中的小蛋白,它的主要功能就是標記需要分解掉的蛋白質(zhì),,使其被蛋白酶體降解,。泛素-蛋白酶體系統(tǒng)是細胞內(nèi)蛋白質(zhì)降解的主要途徑,參與細胞內(nèi)絕大部分蛋白質(zhì)的降解,。
為了驗證這一假設,,研究人員建立了一個人類神經(jīng)元模型系統(tǒng),用以觀察泛素-蛋白酶體系統(tǒng)在阿爾茨海默病發(fā)展過程中的參與情況,。他們發(fā)現(xiàn),,一種被稱為UBB+1的泛素變體會干擾蛋白質(zhì)清除機制的正常運行,從而導致β淀粉樣蛋白沉積(Aβ)和Tau蛋白過度磷酸化的出現(xiàn),,而后兩者是阿爾茨海默病的重要病理標志,。
接下來,研究人員設計了一種特定的核糖核酸(RNA)分子,,這種分子可以抑制UBB+1的表達,。研究人員發(fā)現(xiàn),,抑制UBB+1表達能阻止上述兩種阿爾茨海默病病理標志的出現(xiàn)。
研究人員表示,,研究結(jié)果凸顯了泛素-蛋白酶體系統(tǒng)在清除“缺陷”蛋白質(zhì),、維持細胞健康中的重要性,有助于研發(fā)治療和預防散發(fā)性阿爾茨海默病的藥物,。同時,,相關(guān)RNA分子或可以為治療阿爾茨海默病帶來啟發(fā)。
推薦閱讀

挪威作家約恩·福瑟獲2023年諾貝爾文學獎
新華網(wǎng)2023-10-05 22:21:04
麥卡錫被罷免后把洛佩西“擠”出國會辦公室
新華網(wǎng)2023-10-05 20:21:01
烏克蘭稱又有12艘貨船將進入黑海
新華網(wǎng)2023-10-05 15:21:26
特朗普出庭受審,,因“一再欺詐”面臨2.5億美元處罰
參考消息2023-10-03 14:37:01
迷笛回應“公告言辭粗魯”:符合迷笛風格 不怕事
大眾網(wǎng)2023-10-06 09:41:33
住酒店發(fā)現(xiàn)空調(diào)藏攝像頭報警 店方反稱其團伙作案
北青網(wǎng)2023-10-06 10:17:36
研究稱恐龍注定會滅絕 火山爆發(fā)引發(fā)二氧化碳排放
海外網(wǎng)2023-10-06 11:45:50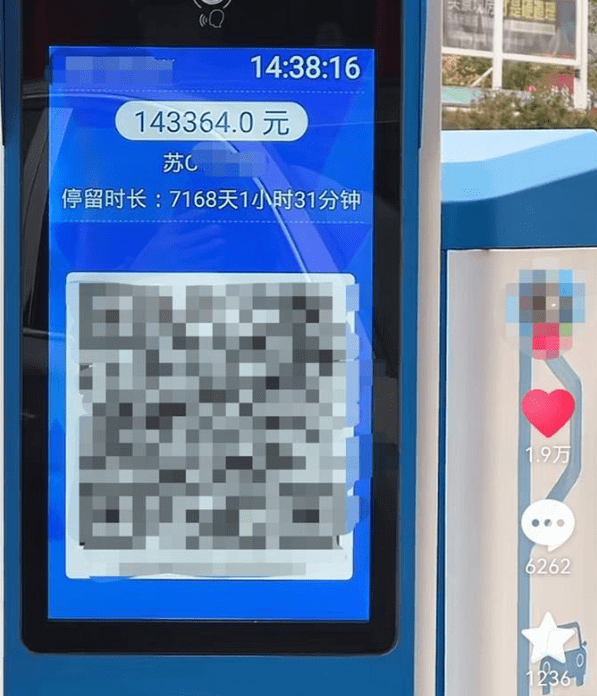
運營方回應“天價停車費”:系統(tǒng)故障 已免費放行
搜狐網(wǎng)2023-10-06 09:01:40
俄黑海艦隊司令接受采訪 他稱艦隊正堅定執(zhí)行任務
環(huán)球網(wǎng)2023-09-28 15:08:22
多元城市音樂會宣布取消:場地安全問題 粉絲炸鍋
2023-10-06 09:50:33
10月1日,,華春瑩連發(fā)11組對比照片,意味深長
觀察者網(wǎng)2023-10-02 18:33:12
梅德韋杰夫警告:西方加碼對烏軍援把世界推向全球沖突
環(huán)球網(wǎng)2023-09-28 11:07:58
俄羅斯:為鞏固對歐洲的控制,,美國炸毀“北溪”
觀察者網(wǎng)2023-09-28 10:40:07
美媒稱美國眾議院陷癱瘓 共和黨“內(nèi)斗”推向高潮
海外網(wǎng)2023-10-06 08:31:39
在黃巖島拆中國的浮動屏障,?菲律賓謊言被拆穿
樞密院十號2023-09-28 10:29:16
中國臺北健兒因觀眾落淚:像自己家人 為我們加油
網(wǎng)易2023-10-06 10:02:20
男子開日料店1年賠180萬 日本排污客流量急劇下降
鳳凰網(wǎng)2023-10-06 11:37:17
馬來西亞總理談5G計劃 華為將能更有效參與
環(huán)球網(wǎng)2023-09-28 15:07:59
煙臺出現(xiàn)新型詐騙模式 假冒保險公司“客服”續(xù)保
煙臺論壇2023-10-06 10:46:24
美媒稱特朗普或于10月2日出席開庭陳述
央視新聞客戶端2023-10-02 18:02:23
本周上班時間有變 六日上班 高速免費6日24時截止
環(huán)球網(wǎng)2023-10-06 08:21:43
俄方談APEC峰會不邀請普京 美方此舉“令人遺憾”
環(huán)球網(wǎng)2023-09-28 11:13:30
俄羅斯考慮效仿中國禁止進口日本水產(chǎn)品,日方稱:沒有科學依據(jù)
環(huán)球網(wǎng)2023-10-02 18:35:30
拜登為罷工工人打氣 “堅持下去”
環(huán)球網(wǎng)2023-09-28 11:15:27
張藝興音樂節(jié)口誤引熱議 眾網(wǎng)友急著為張藝興辯護
搜狐網(wǎng)2023-10-06 11:52:15
特朗普被裁定財務欺詐 特朗普在他的“真實社交”網(wǎng)站上重申,,他沒有什么可自責的
參考消息2023-09-28 13:16:50
梅德韋杰夫:向烏派遣的英國教官將成為俄軍攻擊目標
央視新聞客戶端2023-10-02 18:43:42
美降低退籍費引諸多訴訟 有人要求退還退籍費差價
國際在線2023-10-06 11:07:12
美空軍被曝已退役所有E-8C偵察機,,美媒扯上中俄
環(huán)球網(wǎng)2023-09-28 10:29:57
清華教授差點遭電信詐騙:越來越逼真 防不勝防
環(huán)球網(wǎng)2023-10-06 10:28:27
女子住旅館出小區(qū)被收費 警察來了都沒轍照收不誤
網(wǎng)易2023-10-06 11:13:39
170件武器裝備亮相韓國大閱兵,,韓媒:數(shù)量眾多,,堪稱世界頂級的較少
環(huán)球網(wǎng)2023-09-28 11:31:25
烏克蘭女兵拿到新軍裝 “向北約標準看齊”
參考消息2023-09-28 11:12:22
樂山3名交警10分鐘送醫(yī)游客 警車一路疾馳救治及時
中工網(wǎng)2023-10-06 09:22:28
業(yè)內(nèi)曝楊穎張嘉倪事件被定性,!影響惡劣已開始處理,網(wǎng)友直呼支持嚴懲
ZAKER2023-10-06 08:17:57

















