國產(chǎn)肺癌新藥敲開美市場大門 猛龍過江闖美成功
中國自主研發(fā)的創(chuàng)新藥物舒沃哲(ZEGFROVY,通用名:舒沃替尼片)成功進(jìn)入美國市場。7月3日,迪哲醫(yī)藥宣布該藥獲FDA加速批準(zhǔn)上市,適用于既往經(jīng)含鉑化療治療時或治療后出現(xiàn)疾病進(jìn)展,,并且存在表皮生長因子受體20號外顯子插入突變的局部晚期或轉(zhuǎn)移性非小細(xì)胞肺癌成人患者。

兩年前,,舒沃哲在中國通過優(yōu)先審評獲批上市,,成為全球首個且唯一的EGFR exon20ins NSCLC小分子靶向藥。如今在美國獲批,,標(biāo)志著中國首個獨(dú)立研發(fā)成功出海的全球首創(chuàng)新藥誕生,。第三方機(jī)構(gòu)預(yù)計(jì),舒沃哲有望在全球市場達(dá)到超百億元的銷售峰值,。
迪哲醫(yī)藥創(chuàng)始人,、董事長兼首席執(zhí)行官張小林表示,相對于國內(nèi)市場,,歐美市場支付能力更強(qiáng),,海外市場有望成為公司業(yè)績增長的新動力。根據(jù)《Front Immunol》文章,,EGFR基因20號外顯子插入突變在中國非小細(xì)胞肺癌患者中的發(fā)生率約為4.8%~5.1%,,是公認(rèn)的“難成藥”靶點(diǎn)。目前,,臨床針對該靶點(diǎn)的一線治療仍以化療為主,,傳統(tǒng)EGFR小分子靶向藥和免疫治療均未攻克此突變。
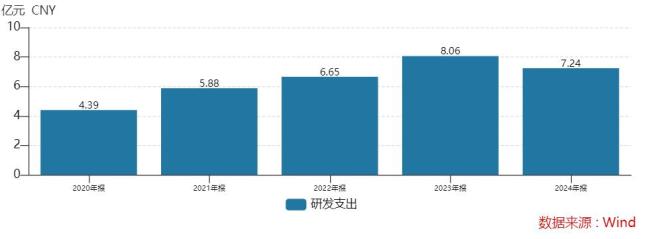
舒沃哲作為國內(nèi)唯一獲批且可醫(yī)保報銷的EGFR exon20ins NSCLC二/后線標(biāo)準(zhǔn)治療方案,,被市場寄予厚望,。中航證券研報顯示,根據(jù)2019年新發(fā)病例數(shù)量測算,,舒沃哲中國市場銷售峰值有望達(dá)到30.76億元,。在美國獲批上市意味著新的市場增量,尤其是考慮到海外抗腫瘤藥物定價普遍為中國的一倍左右,商業(yè)化價值更高,。按照中航證券預(yù)計(jì),,舒沃哲全球市場銷售峰值有望達(dá)到129.54億元。
迪哲醫(yī)藥正在積極評估各種海外市場拓展模式,。張小林指出,,中美醫(yī)藥市場格局不同,公司將遵循美國市場特點(diǎn)制定相應(yīng)策略,。公司定位參與全球化競爭,,以長遠(yuǎn)發(fā)展為目標(biāo),最大化公司利益并為股東創(chuàng)造更多投資回報,。海外市場有望成為公司業(yè)績增長的重要部分,,但國內(nèi)市場仍是重要陣地。在舒沃哲納入醫(yī)保之后,,公司2025年一季度收入規(guī)模同比增幅近100%,。今年將全力提升醫(yī)保產(chǎn)品的市場覆蓋率,目前的商業(yè)化團(tuán)隊(duì)已接近500人,。
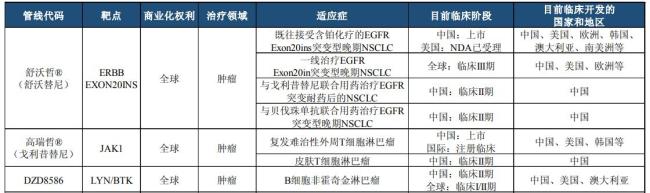
迪哲醫(yī)藥的核心團(tuán)隊(duì)成員來自原阿斯利康亞洲研發(fā)中心,,公司成立伊始就錨定全球競爭,所有管線從臨床I期開始即全球同步開發(fā),,均享有完整全球權(quán)益,。2024年年報顯示,公司處于國際多中心臨床階段的管線共有7條,,進(jìn)展最快的產(chǎn)品包括舒沃哲,、高瑞哲(通用名:戈利昔替尼),、DZD8586和DZD6008,。
公司在肺癌和血液瘤領(lǐng)域形成接力布局。張小林表示,,公司的研發(fā)團(tuán)隊(duì)在這些領(lǐng)域有深厚的積累,,因此聚焦這兩個領(lǐng)域,在具有差異化優(yōu)勢的領(lǐng)域進(jìn)行全球競爭,。DZD6008是迪哲醫(yī)藥自主研發(fā)的一款高選擇性EGFR TKI,,在三代EGFR TKI和多線治療失敗及腦轉(zhuǎn)移的病人中顯示優(yōu)異的安全性和有效性,有望填補(bǔ)NSCLC領(lǐng)域未滿足的臨床需求,。
舒沃哲單藥一線治療EGFR exon20ins NSCLC經(jīng)確認(rèn)的客觀緩解率達(dá)78.6%,,中位無進(jìn)展生存期為12.4個月,有望進(jìn)一步重塑該領(lǐng)域一線治療格局,。近期,,舒沃哲一線治療EGFR exon20ins NSCLC的全球多中心Ⅲ期臨床研究“悟空28”已完成全部患者入組。
在血液瘤領(lǐng)域,已上市產(chǎn)品高瑞哲是全球首個且唯一針對外周T細(xì)胞淋巴瘤的高選擇性JAK1抑制劑,,打破PTCL“全球十年無創(chuàng)新藥”困局,,是目前單藥治療該類患者的中位總生存期最長的藥物,首次突破2年以上,。DZD8586則是全球首創(chuàng)的非共價LYN/BTK雙靶點(diǎn)抑制劑,,能全面阻斷BCR信號通路,并完全穿透血腦屏障,,針對多種B細(xì)胞非霍奇金淋巴瘤展現(xiàn)出良好抗腫瘤活性,。
迪哲醫(yī)藥將繼續(xù)擴(kuò)展適應(yīng)證,隨著投入更多的臨床研究,,臨床適應(yīng)證會逐步擴(kuò)大,,其臨床和商業(yè)價值會不斷體現(xiàn)。公司計(jì)劃將超過10億元的募投資金投向新藥研發(fā)項(xiàng)目,,主要用于舒沃替尼,、戈利昔替尼、DZD8586的臨床研究,。張小林強(qiáng)調(diào),,盡管ADC、雙抗,、細(xì)胞治療等是中國創(chuàng)新藥的優(yōu)勢領(lǐng)域,,但迪哲醫(yī)藥的研發(fā)決策建立在對臨床未滿足需求的深刻理解和轉(zhuǎn)化科學(xué)的基礎(chǔ)之上,選擇自身能形成高技術(shù)壁壘的小分子藥物設(shè)計(jì)領(lǐng)域,,而非追趕當(dāng)前行業(yè)熱點(diǎn),。
相關(guān)新聞
國產(chǎn)流感創(chuàng)新藥進(jìn)入井噴期 多款新藥即將上市
2025-03-04 21:14:21國產(chǎn)流感創(chuàng)新藥進(jìn)入井噴期首個國產(chǎn)TED靶向新藥上市 打破70年無新藥困境
2025-03-21 18:16:27首個國產(chǎn)TED靶向新藥上市2025國產(chǎn)創(chuàng)新藥“出?!苯輬箢l傳 交易額破百億美元
2025-02-18 11:44:492025國產(chǎn)創(chuàng)新藥出海捷報頻傳上海造“超長續(xù)航”降糖藥獲批 國產(chǎn)新藥開啟治療新篇章
2月11日,,上海銀諾醫(yī)藥自主研發(fā)的GLP-1糖尿病新藥怡諾輕(依蘇帕格魯肽α)在上海市第六人民醫(yī)院和江蘇省南京鼓樓醫(yī)院兩地開出全國首張?zhí)幏?/a>
2025-02-16 19:06:41上海造超長續(xù)航降糖藥獲批國產(chǎn)創(chuàng)新藥為全球提供“中國方案” 重構(gòu)醫(yī)藥競爭格局
國內(nèi)藥企通過不斷提升的研發(fā)創(chuàng)新能力,,正以前所未有的速度與決心走向國際市場,為世界提供更多“中國方案”
2025-06-13 11:43:47國產(chǎn)創(chuàng)新藥為全球提供中國方案創(chuàng)新藥概念股逆勢大漲 醫(yī)藥板塊領(lǐng)漲市場
2025-05-30 12:27:33創(chuàng)新藥概念股逆勢大漲